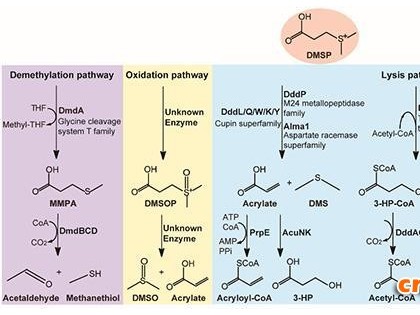
中国科学院成都生物研究所吴中柳课题组研究人员将羰基还原酶READH和苯乙烯单加氧酶StyAB共表达于大肠杆菌E. coli BL21-ΔnemA,构成了一个多酶偶联体系:首选a,b不饱和酮经羰基还原酶READH还原成烯丙醇,后者被苯乙烯环氧化酶StyAB选择性环氧化后,再经羰基还原酶READH脱氢生成环氧酮。在这个过程中,还原型辅酶得到再生,从而构成一个自给自足的反应体系,有效催化缺电子的a,b-不饱和酮生成多种(3S, 4S)-4-苯基-3,4-环氧-2-丁酮衍生物,具有优异的对映体选择性和转化率。若在反应体系中添加适量异丙醇则特异性地生成具有三个连续手性中心的(2R, 3S, 4S)-4-苯基-3,4-环氧-2-丁醇类衍生物。该方法首次解决了不饱和酮的生物催化不对称环氧化这一难题,为绿色催化提供了新的思路。
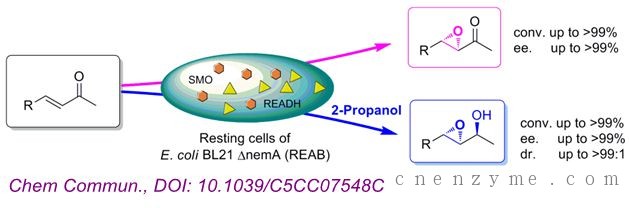
合成路径
本研究成果发表在Chem. Commun. 2016, 52(6), 1158 – 1161.