摘要:甘露聚糖酶是一种新型的促生长饲料添加剂。本试验初步研究了康地恩甘露聚糖酶的最适反应pH及反应温度、酶的湿热稳定性、pH稳定性,以上酶学性质研究的数据表明,该酶的活性较高,在饲料工业中具有很好的应用前景。
关键词:甘露聚糖酶;酶活;性质;饲料
甘露聚糖酶是一种半纤维素水解酶,以内切方式降解β-1,4糖苷键,降解产物的非还原末端为甘露糖,其作用底物包括葡萄甘露聚糖、半乳甘露聚糖及β-甘露聚糖等。它不仅能够降解肠道粘度,促进营养物质的消化和吸收,而且还可消除豆类中富含的β-甘露聚糖对葡萄糖吸收的干扰,极大提高饼粕尤其是豆粕的能量消化率;同时,添加了甘露聚糖酶后动物的抵抗力及整齐度都有提高。
甘露聚糖类物质作为半纤维素的第二大组分,广泛分布于自然界中。它是所有豆科植物细胞壁的主要组成成分,在其他植物性饲料原料中含量也很高,如豆粕、小麦、菜籽粕、麸皮中半乳甘露聚糖占非淀粉多糖的含量分别为22.7% ,11.9% ,19.6%和33.7%。
我国猪、鸡的主要日粮是玉米/豆粕型日粮,尽管猪、鸡等单胃动物对玉米的消化率较高,但对豆粕的能量利用率仅为50%~60%。单胃动物对豆粕能量的利用率如此低的原因可能是豆粕中含有22.7%左右的半纤维素是不能被单胃动物消化的非淀粉多糖。饲料中添加甘露聚糖酶可以降解甘露聚糖、降低消化道内容物黏度,破坏植物性饲料细胞壁结构,使营养物质能与消化酶充分接触,提高内源酶的活性,改善肠道微生物菌群和提高肠粘膜的完整性等功能。
本文旨在通过对康地恩甘露聚糖酶的酶学性质研究,掌握有关数据,为实际应用提供理论依据和指导。
1材料与方法
1.1 材料与试剂 康地恩甘露聚糖酶;甘露聚糖(Sigma公司);3,5—二硝基水杨酸(DNS);甘露糖(Sigma公司)。
1.2 主要实验仪器 722型分光光度计;电子分析天平;可调恒温水浴锅;精密pH计等。
1.3 酶活力测定
1.3.1酶活测定方法。采用还原糖法(DNS)测定。
1.3.2 酶活力单位定义。在40℃、pH4.5的条件下,每分钟从甘露聚糖(Sigma G0753)溶液中降解释放1 μg还原糖所需要的酶量为一个酶活力单位U。
1.3.3甘露糖标准曲线的绘制。配制10mg/mL的甘露糖溶液100mL,吸取上述溶液分别配制成浓度为0.10~0.70 mg/mL的甘露糖标准溶液。
分别吸取上述浓度系列的甘露糖标准溶液各2.00mL(做二个平行),加入到刻度试管中,再分别加入2.00mL蒸馏水和5.00mL DNS试剂,(标准空白测定则是以2.00mL蒸馏水代替甘露糖标准溶液),电磁振荡3s,沸水浴加热5min,然后用自来水冷却到室温,再用水定容至25mL。以标准空白样为对照调零,在540nm处测定吸光度OD值。
以甘露糖浓度为Y轴、OD540为X轴,绘制标准曲线。
1.3.4 酶活力的测定。吸取2.00mL经过适当稀释的酶液,加入到刻度试管中,预热2min,再加入2.00mL经过预热的甘露聚糖溶液,电磁振荡3s,恒温反应30min。加入5.00ml DNS试剂,电磁振荡以终止酶解反应。沸水浴加热5min,用自来水冷却至室温,加水定容至25mL,混合均匀。同时采用先加DNS试剂后加甘露聚糖溶液的酶液为空白对照,在540nm处测定吸光度。吸光度控制在0.2~0.4范围内。
1.4 实验方法
1.4.1 酶反应的最适pH。配制A :0.05mol/L的柠檬酸溶液,B:0.1mol/L的磷酸氢二钠溶液,将A、B两种溶液按一定比例混合配制pH分别为2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5的缓冲液;以蒸馏水配制0.8%的甘露聚糖溶液,酶样品用蒸馏水稀释50倍后再以不同pH的缓冲液作适当稀释进行酶活测定。以最高酶活为100%,在其他条件的酶活占最高酶活的百分数即为该酶在此pH条件下的相对酶活。
1.4.2 酶反应的最适温度。调节恒温水浴锅,分别设定反应温度为30℃、35℃、40℃、45℃、50℃、55℃、60℃、65℃、70℃,在最适pH缓冲液下测定酶活,以最高酶活为100%,在其他条件的酶活占最高酶活的百分数即为该酶在此温度条件的相对酶活。
1.4.3 酶的湿热稳定性。称取5.0000g左右酶样品,以对应最适pH的缓冲液定容至50mL,搅拌30min,以4000rpm离心10min,取上清液待用。将两支盛有9mL最适pH缓冲液的试管分别在40℃、50℃、60℃、70℃、80℃、90℃的水浴锅中预热10min,分别加入1.00mL酶液迅速摇匀并准确计时2min、5min,取出后迅速于冰水浴中冷却后于最适pH和温度40℃的条件下测定酶活,以未经高温处理的酶样酶活为100%,其他条件的酶活占未处理酶样酶活的百分数为相应条件的相对酶活。
1.4.4酶的pH稳定性(耐酸性)的研究
1.4.4.1称取1.5000g酶样加入15mL保护液(2%葡萄糖+2%牛肉膏+2%蛋白胨)在磁力搅拌器上搅拌30min,在最适pH和温度40℃的条件下测定酶活作为对照。
1.4.4.2称取1.5000g左右酶样品十二份,分别加入15mL保护液,搅拌30min,以合适浓度的柠檬酸溶液(0.3mol/L)或氢氧化钠溶液(3mol/L)调pH分别至2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0,准确记录所用柠檬酸或氢氧化钠溶液的体积Va1~Va12,再用相同浓度的氢氧化钠溶液或柠檬酸溶液调整pH至该酶的最适pH,同样记录所用溶液的体积Vb1~Vb12。
1.4.4.3称取1.5000g左右酶样品十二份,分别加入15mL保护液,搅拌30min,于40℃水浴锅中预热10min,于磁力搅拌器上边搅拌边迅速加入1.4.4.2中记录体积Va1~Va12的柠檬酸或氢氧化钠溶液于水浴锅中保温(加入柠檬酸或氢氧化钠溶液即开始计时)2h;结束后,在磁力搅拌器上边搅拌边迅速加入1.4.4.2中记录体积Vb1~Vb12的氢氧化钠或柠檬酸溶液,在最适pH和温度40℃的条件下测定酶活,以1.4.4.1所测酶活为100%,其他条件的酶活占对照酶样酶活的百分数为相应条件的相对酶活。
2 结果与分析
2.1 甘露聚糖酶的最适反应pH
在40℃、不同pH的缓冲液中测定酶活见图1。
由图1可以看出,康地恩甘露聚糖酶随着pH的增加,酶活呈上升趋势,在pH4.5时达到高峰,然后开始下降,在pH3.0~5.5之间可保持80%以上的酶活。同样得到另外几种样品的最适pH分别为:市场样A6.5、市场样B5.5、市场样C6.5、甲公司07年样品5.5、甲公司06年样品6.0、某公司样品A和样品B均为5.0。
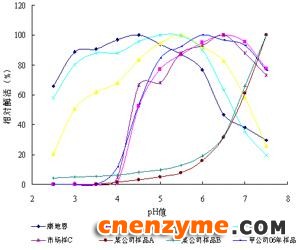
图1 pH值对各种甘露聚糖酶活的影响
2.2 甘露聚糖酶的最适反应温度
调各甘露聚糖酶液pH为其最适反应pH,在不同温度下测定的酶活变化情况见图2。
由图2可以看出,康地恩甘露聚糖酶酶活随着反应体系温度的增加呈上升趋势,到70℃酶活达到最高,温度超过70℃后酶活开始下降,该酶的最适反应温度为70℃;同样由图可以得到另外几种样品的最适反应温度分别为市场样A50℃、市场样B65℃、市场样C45℃、甲公司07年样品70℃、甲公司06年样品50℃、某公司样品A60℃。
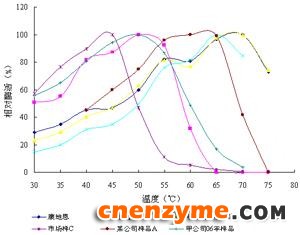
图2 温度对各种甘露聚糖酶活的影响
2.3甘露聚糖酶的湿热稳定性
经不同温度分别湿热处理2min及5min后酶活变化曲线如图3。
由图可以看出,各甘露聚糖酶在湿热处理2min及5min后酶活曲线基本具有相同的变化规律。在40℃~60℃康地恩甘露聚糖酶酶活基本无差异。温度在76℃以下时保持80%以上的酶活。市场样A随着温度升高酶活逐步下降,温度58℃时酶活已降至80%以下,70℃已无酶活。市场样B在40℃~60℃酶活变化很小,然后随着温度升高酶活逐步下降,温度72℃时已降至80%以下。甲公司07年样品随着温度升高酶活逐步下降,温度64℃时酶活已降至80%以下。
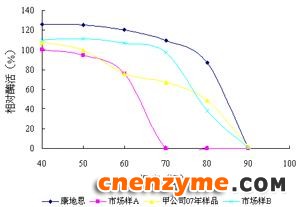
图3(1)各甘露聚糖酶经不同温度湿热处理2min后酶活变化情况
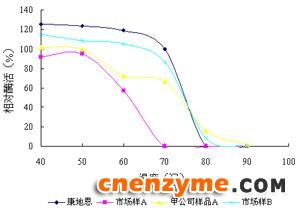
图3(2)各甘露聚糖酶经不同温度湿热处理5min后酶活变化情况
2.4 pH稳定性的研究
经不同的pH条件处理2h后,酶活变化曲线如图4。
由图可以看出,康地恩甘露聚糖酶在pH3.0~8.0之间的环境中2h处理后酶活较稳定,一直保持在80%以上;市场样A在pH小于5.0的环境处理后酶活不稳定,在pH5.0~8.0之间的环境中2h处理后酶活一直保持在80%以上;市场样B在pH小于4.0时,酶的剩余活力较低,在pH4.0~8.0时酶活基本不受环境影响;甲公司07年样品在pH小于4.0时,酶的剩余活力较低,在pH4.5~8.0时,酶活较稳定。
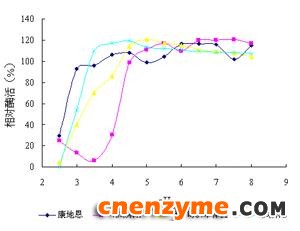
图4 各甘露聚糖经不同的pH处理后酶活变化情况
3结论
文章通过对康地恩甘露聚糖酶酶学性质的研究分析可以对酶的基本性质有了比较详细的了解,该酶的最适反应pH为4.5,最适反应温度为70℃;该酶具有较强的湿热耐热性,不同温度下分别湿热处理2min及5min后发现在40℃~60℃酶活基本无差异,温度在76℃以下时保持80%以上的酶活;该酶的pH稳定范围较宽,经不同的pH条件处理2h后,在pH3.0~8.0之间的环境中酶活较稳定,一直保持在80%以上。这些数据表明该酶具有极佳的适合饲料工业用的酶学性质,酶的活性较高,在饲料工业中有很好的应用前景。
参考文献
[1] 李富伟,周响艳.饲用β-甘露聚糖酶的研究及应用[J].饲料工业,2007,28(2):16~19
[2] 刘朝伟,武伟娜.保护剂提高β-甘露聚糖酶热稳定性的研究[J].天津大学学报,2008,41 (1):114~118
[3] 马延和,田新玉.碱性β-甘露聚糖酶的产生条件及一般特性[J].微生物学报,1991,31(6):443~448
[4] 杨文博,佟树敏.地衣芽孢杆菌β-甘露聚糖酶的纯化及酶学性质[J].微生物学通报,1995,22(6):338~342
[5] Christgau S, Kauppinen S. Vind J, et al. expression cloning, purification and characterization of a beta-1,4-mannanase from Aspergillus aculeatus[J]. Biochem. Mo1. Bio. Int,1994,33(5): 917~925
[6] McClearyB v.B-mannanase[J]. Methods in Enzymeology,1988,160:596~610




